榮格工業資源APP
了解工業圈,從榮格工業資源APP開始。
引言
早在二十年前,可提取物與浸出物就成為了合格醫藥包裝材料(以下簡稱藥包材)的首要選擇。藥包材是藥品的一部分,由于藥包材的組成配方、原輔材料及生產工藝的不同,有些組分可能存在向內容物(藥品)產生遷移、與藥品發生反應或被藥品長期浸泡,腐蝕脫片而直接影響藥品質量的現象,進而產生安全隱患。中國則是在2004年7月20日,由原國家食品藥品監督管理局發布了《直接接觸藥品的包裝材料和容器管理辦法》,強化了藥包材標準的管理,加大了對藥包材監督管理力度。2012年1月,國務院發布的《國家藥品安全“十二五”規劃》中明確提高139個直接接觸藥品的包裝材料標準,制訂100個常用直接接觸藥品的包裝材料標準。去年8月,我國CFDA又發布了YBB 00032005-2015《鈉鈣玻璃輸液瓶》等130項直接接觸藥品的包裝材料和容器國家標準的公告(2015年第164號)。這些政策都進一步督促藥品制劑企業切實承擔藥用輔料和藥包材的相容性研究,確保產品質量安全。
然而隨著藥品及其給藥系統的復雜性日益增加,給確認和定量檢測浸出物帶來了極大的挑戰。盡管存在針對可提取物與浸出物的管理規定,但是它們只為確保病人安全提供了一般性的建議。按部就班的指導是不切實際的,因為各個產品的劑型、構造材料、結構和用量都各不相同。因此,有可能給病人造成的影響必須具體問題具體分析。現代的產品生產質量管理規范 (GMP) 倡導在藥品研發之初就采用基于風險的方法,確定浸出物的潛在可能應該是確保病人安全的當務之急。針對浸出物的綜合性研究是對產品建議保質期內有可能從包裝材料遷移到藥品當中的成分進行定性及定量評估。存在的問題包括:需要進行多少次測試;什么時候以及在什么靈敏度下;如何為限制條件確定流程。在食品、藥品和醫療器械行業,提取接觸材料的方法和對提取物進行評估都已廣泛應用,它們的共同目標是了解哪些成分會從這些材料里遷移出來并可能造成危害。雖然我們希望有明確的方法以及確定的靈敏度和規格,能夠適用于所有情況,但這是不切實際的。本文將著眼于可提取物和浸出物技術,并對相應的方法、應用和基于風險的策略展開討論。
背景
可提取物指當有溶劑存在時那些可以從容器密封系統的組件中遷移出來的化合物。這些可提取物有可能變成浸出物,即在存儲過程中隨著時間推移可以從容器密封系統遷移到劑型當中的化合物。對在藥品的生產、封裝和運輸過程中與藥品有直接或間接接觸的組件評估其在所有劑型中產生的潛在浸出物是非常重要的。醫藥保健行業的不少人都還記得1990年的幾起事故,主要是2,4,6- 三溴苯甲醚和2,4,6- 三氯苯酚遷移到藥片當中,原因就是間接接觸的運輸托盤產生的分子擴散和滲透。 據報道,形形色色的生物蛋白產品都遭遇了各種不同的浸出物事故,涉及源于內包材和預灌注注射器的金屬陽離子、鎢、溴、丁羥甲苯和有機溶劑。 為了確保進入擴大規模和商業階段時的信心,制藥企業應當在藥品研發過程中識別出浸出物成分,并對它們有可能給藥品和病人造成的影響進行評估。對包裝組件進行評測,能夠獲得在藥品整個生命周期確定質量控制點所需要的信息。對于這些組件的應用而言,質量控制點是明確而具體的。不幸的是,在研發早期,包裝形態、制藥過程、劑型配方以及給藥劑量均無法完全確定,而他們都有可能對浸出物產生影響。 對這些組件逐一進行評測,其程度和類型取決于諸多相關因素。制藥和醫療器械行業采用了多種類型的材料,如表1所示:劑型、材料和相關風險示例。所有類型的材料都有可能產生浸出物。金屬、玻璃、橡膠和塑料會給病人安全和藥品質量帶來風險。與產品直接接觸的材料(比如玻璃或不銹鋼)中成分的浸析和脫落,產生顆粒物,會影響藥品的純度和安全性。 高分子材料有面臨這樣的風險——同藥品直接或間接接觸的組件材料中的成分可能會遷移出來,遇熱或有溶劑存在時尤其如此,所以應當嚴格評測。
遷移的原理
對于可提取物導致產生浸出物的可能性,可以通過以下幾個方面來觀察:與揮發成分滲透進藥品相關的遷移物交互反應;遷移物在包裝產品界面上的累積,然后分裂進入藥品或沉淀物。遷移現象由一系列的物理和化學過程組成,包括可提取物的擴散速度、溶解度、滲透作用和化學結構。暴露面積會影響到它們是否有可能發生遷移。時間、溫度和接觸介質/溶劑類型也可能影響遷移速度。最后,產品保質期內的實際暴露將成為影響病人安全的證據,因為它關系到浸出物的積累和每天的給藥劑量。盡管可能采用了預測模型,仍有很多因素會導致多組分體系,預測模型在其中會導致極大的不確定性。此外,在有些情況下,提取模型研究并不能捕捉到所有潛在的浸出物,或者不能完全代表最大濃度。為保證病人安全,需要對提取實驗進行很好的設計并實施,然后再進行全面的保質期內浸出物研究。
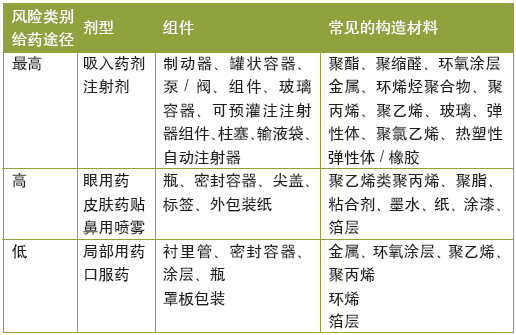
表 1 劑型、材料和相關風險的示例
在制造和生成諸如添加劑、加工助劑、殘余物和清潔劑之類材料過程中用到的原料都有可能成為可提取物,從而導致污染或降解產物。進行一次對照提取實驗,這是有可能識別出浸出物的第一步。這些實驗應該包括在最后的加工 ( 比如滅菌和組裝) 之后進行提取操作,揭示那些潛在的浸出物,因為這個系統將在產品保質期內與藥品直接接觸。美國和歐洲對高分子材料中添加劑的遷移以及對食品安全的影響進行了廣泛的研究。此外,還頒布了法律,列出了準許使用的間接食品添加劑清單,以此來保護消費者。一些監管法令為安全性規定了門檻限制值,也就是允許在生產包裝材料過程中添加的數量,有時還規定了具體的遷移限制值。門檻限制值對浸出物評測是很重要的,但說到要確定包裝是否可供醫藥制品使用,食品添加劑監管規定所列出的規格作用有限。在制藥和醫療器械行業,相關的添加劑或源自聚合物的化學成分的遷移,考慮采用其他暴露途徑和影響評測,這些評測不一定產生同樣類型的警告類型。
一旦通過操作得當的實驗確認了浸出物,就可以對其給病人和醫療產品產生的影響進行評測。有許多預料得到的物質也可能浸出,但只有那些超過可接受水平的浸出物才在我們的考慮范疇之內。產品質量研究所為口服吸入產品和鼻用藥物給出了浸出物的安全門檻值;其他劑型的門檻值仍在研究當中。識別浸出物并為其劃分重要等級有賴于全面了解包裝組件的化學屬性;但是,僅僅只有可提取物的數據,是無法預測對病人的影響的。了解組件的化學屬性和遷移的機理,有助于制定適當的可提取物和浸出物方法,從而為基于科學的控制策略提供理論依據。
可提取物可以按照分子量和其他方面的屬性進行劃分,通過考量影響遷移的參數從而與提取的可能性關聯起來。這種信息有助于找到適合的實驗方法。對于那些有證據表明具有毒性的成分而言,既定浸出物的潛在安全影響是最大的,但它們通常只是微量存在,并非時時便于檢測。潛在浸出物的類別表明了遷移物潛在的擴散性;為了制定分析方法,應當考慮導向針對化學物質展開適當研究的表面相互作用。 潛在浸出物的影響因素如表2所示:潛在浸出物的物理及化學指標。
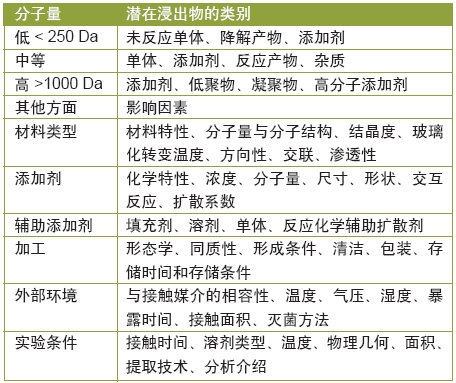
表 2:潛在浸出物的物理及化學指標
可提取物
關鍵組件 ( 生產和封裝用到的組件或者與藥品接觸的其他材料) 的選擇和實驗材料的提取是進行可提取物實驗的基礎。為了全面了解可提取物,對組件適當取樣是必不可少的,像微量成分的變異性就是不能忽略的。而且,要想得到正確的數據,適當的樣品制備、材料轉化為溶劑的比率、溶劑類型和提取條件都是至關重要的。關鍵組件的功用以及對組件構成和藥品配方的了解都應該用于指導我們選擇合適的溶劑。此外,應該采用多種不同的提取方法和分析方法。 應該好好計劃實驗過程,以期得到的結果不僅能支持實驗目標,還能促成浸出物實驗。可提取物評估有多種用途,比如全面的化學特性鑒定分析,以了解它們在嚴苛條件下或模型系統中變成浸出物的可能性,指出其預期用途,從而揭示其在指定條件下浸析的可能性。模型系統是為了在加速情況下對產品進行模擬,通常應用于食品行業和某些醫療器械的制造。 , 無論提取實驗選擇什么樣的條件,實驗結果應該將醫藥包裝中的浸出物的類型和數量彼此關聯并證實。這些信息是評判病人安全所需要的。
為了與模擬遷移的加速條件下的化學特征進行對比,圖1給出了為聚丙烯樣本產生的數據示例:材料特性GC/MS數據與模擬實際使用條件下GC/MS數據的對比,進行特性鑒定分析的條件所提供的信息有助于通過遷移物的最大化了解可提取物的化學特性,因為模型提取實驗采用了用于展示或預測實際用途的模擬條件。GC/MS色譜圖告訴我們:單單就模擬條件而言,還不能提供足夠的信息,幫助我們了解可提取物的綜合概況或進行浸出物評測。但是,它們可以用作評測遷移行為的標尺。
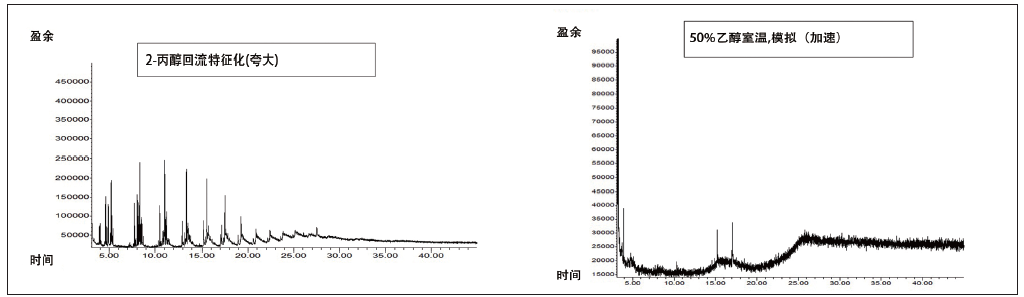
圖 1:材料特性 GC/MS 數據與模擬實際使用條件下 GC/MS 數據的對比。
提取物的產生以及可提取物或遷移物質的識別和測定都是相當耗時的,應該采用系統性的實驗方法。了解遷移行為,可以幫助我們更明智地選擇實驗參數和分析方法。要考量的聚合物特性包括:
? 高分子效應 ( 形態學、分子結構表面能、熵) ;
? 化學成分的有形損失和轉化為相關的降解產物;
? 復雜混合物內的化學反應、副產品或反應產物;
? 化學物質遷移到表面;
? 接觸媒介中的溶解性、沉淀物、暈染效應;
? 基于分子運動 ( 擴散速度或揮發) 的提取物損失和質量傳遞;
? 頂部空間的釋氣 ( 剩余成分的蒸發) 或溶液中的積累;
? 滲透性或化學物質通過材料轉移。
浸出物
浸出物實驗通常在藥物開發的后期階段進行。在這些實驗當中,藥品在各種受控的環境條件下穩定地存儲,并在藥品預定保質期內的多個時間點接受定性和定量分析。 可提取物是潛在浸出物的一個標志,但藥品中化學單體遷移的可能性是無法預料的,進行得非常緩慢, ( 或者) 在獨特且無法預料的條件下才會發生。當影響遷移的參數 ( 比如溫度) 被加速,則有可能出現異常。如果環境或接觸媒介太過潮濕,都有可能捕捉不到浸出物。藥品雜質分析可能會檢測出浸出物,不過通常濃度很高,有必要進行獨立的實驗來追蹤,并將它們同源頭關聯起來。這里給出了一個在為眼科用品開展的雜質分析中檢測到浸出物的示例。Changkang 描述了為 0.19% 的雜質追蹤到源頭——涂漆的方法。 為了減少追蹤異常或錯失關鍵浸出物的風險,應該在穩定期間進行針對性實驗,因為早期評估可以提示潛在危險。藥品的穩定性是在需要其研發階段和整個生命周期監測的關鍵屬性,但不能始終對雜質測定實驗進行優化,以使潛在浸出物達到適當的濃度。藥品降解產物、雜質和潛在浸出物都需要適當的方法來發現和測定。微量成分可能有多個來源,( 或) 來源不明。浸出物方法應當足夠穩健,能夠捕捉到意料之中的、意料之外的以及潛在的未知物質。因為方法可能非常敏感,要識別未知物質及其源頭就具有相當的挑戰性。可以投入大量的時間來隔離并確認這些未知的浸出化合物。綜合性的可提取物實驗應當讓我們更好地了解組件的化學特性,并有利于識別未知的浸出化合物及潛在的反應機理。
一旦可以從可提取物或遷移物的角度去了解與藥品接觸的材料,就應當對潛在的浸出物進行評測。有必要做出決定和選擇——在觀測的化學物質當中,哪些關系到病人安全和藥品質量。浸出物實驗必須在分析浸出物之前進行多個步驟:明確識別化合物;為測定準備好參考物;設置好適當的儀器和分析條件;進行驗證和優化以具備足夠的敏感度。可以預見的是,這個藥品“矩陣”會影響檢測方法和分析物的回收。藥物配方中的成分通常會掩藏濃度較低的成分的反應或者依附到基質上,這同樣會帶來問題。有的針對性研究在明確的基質中采用經過優化或驗證的方法來測定浸出分析物,可以得到有關浸出物的更為準確的信息。為了目標分析物在基質內適當的特異性、回收率和再現性而制定的方法,可以為與可提取物相關的浸出物實驗奠定基礎。
采用一種理論方法,并 ( 或) 在模擬或嚴苛環境下進行提取實驗,可以在可提取物和浸出物之間搭起一座“橋梁”。評測結果提供的背景信息可以確保制定出適當的浸出物方法或表現出潛在的毒理學關注。這些數據研發早期都能發揮一定的作用,尤其是在具體的藥品配方還沒有最后確定的時候。最能逼真模擬藥品基質、安慰劑或藥品本身的溶劑通常都在加速條件下被使用。通常而言,方法優化對于在復雜基質中進行加速試驗是必需的,這些實驗可能生成浸出物,也可能不行。材料特征的鑒定分析以及通過具體方法的制定和在整個穩定期間對浸出物進行監測來了解可提取物并非一個漫長的過程,但它是一個遵循 “質量源于設計” (QbD) 原則的過程。
QbD的目標是基于目標藥品的質量概況 (QTPP) 為質量屬性進行規劃。與劑型接觸部件的質量概況應該包括浸出物的可接受濃度水平。浸出物的風險應與劑型屬性、給藥途徑、病人數量、給藥劑量和病人的每日用量關聯起來進行評測。背景知識有助于為回收和了解源自綜合性可提取物評估的潛在浸出物提供指導。應該基于浸出物實驗、現有產品和工藝理解來制定一套有計劃的控制方法,在考慮病人安全的前提下確保產品質量。
小結
了解可提取物的原理,并使用基于風險的策略與浸出物相互關聯,不僅可以在藥品研發階段提供支持,這種支持還一直延續到藥品的整個生命周期。應用基于風險的策略可以提供理論依據,影響決策,從與劑型直接或間接接觸的材料這一方面確保藥品質量和病人安全。最后的組件選擇和藥品配方設計應該考慮在材料特征分析鑒定試驗和風險評估中得來的信息,以便降低之后藥品配方研制過程中的風險。
可提取物和浸出物的實驗方法各不相同,取決于具體的產品和病人的給藥途徑。在模擬條件下產生的提取物可用于將可提取物實驗與浸出物實驗關聯起來,但也有一定的限制,不應被視為單一的浸出物實驗。根據風險和具體方法的制定來選擇目標浸出物,在藥品保質期內對浸出物進行檢測,這是符合QbD原則的。對浸出物進行準確的測量和評估 ( 方法經過充分驗證) 是保證藥品質量和病人安全的關鍵要素。中國制藥業目前也正經歷由“質量源于檢測”向“質量源于設計”的悄然轉變,制藥企業需要盡快運用QbD原則進行藥物開發,以便更好得應對市場和客戶對于醫藥包裝日趨繁復、多變的需求。
參考文獻:
1. 美國注射劑協會 (PDA) 通訊,《運輸托盤:看似干凈,其實很臟》,第 48 卷,第 5 期,第 30 頁,2012 年 5 月:http://www.pda.org/Publications
2.Markovic, I.,《治療性生物蛋白產品中可提取物與浸出物安全認證的風險管理策略》,發表于《美國藥物評論》,2009 年6 月。
3.Bak, A.,《藥品發現:對從發現過渡到開發這一過程進行管理的科學風險評估策略》:AAPS Newsmagazine,2010 年 7 月,http://www.nxtbook.com/nxtbooks/aaps/newsmagazine
4. 人類用藥和生物制品的包裝容器密封系統,CMC 文檔、CDER/CBER/FDA 行業指南 (1999 版),http://www.fda.gov
5. Paskiet D.,《注射用藥產品中浸出物的評估策略》,PMP,2008。
6. Markovic, I., CDER/FDA 《治療性生物蛋白產品中可提取物和( 或) 浸出物相關的挑戰》。《美國藥物評論》,2007 年 5 月,http://www.americanpharmaceuticalreview.com
7. 美國食品和藥物管理局,聯邦法規第 21 篇第 170-199 部分,美國國家檔案文件管理局《聯邦公報》處;http://www.accessdata.fda.gov
8. 歐共體,第 2002/72/EC 號歐盟指令,《關于與食物接觸的塑料材料和物品》,http://ec.europa.eu/food/food/chemicalsafety/foodcontact/legisl_list
9. 產品質量研究所 (PQRI) 研究項目計劃書:注射用藥和眼科用藥中浸出物門檻值的報告與評定:2007, http://www.pqri.org
10. 產品質量研究所 (PQRI),浸出物與可提取物工作小組,《口服吸入藥和鼻科用藥中可提取物與浸出物的安全閥值與最佳實踐》。2006 年11 月,http://www.pqri.org
11. Bart J.C J;《高分子添加劑分析》發表于《行業實踐與案例分析》,佛羅倫薩大學出版社,2006 年。
12. 產品質量研究所 (PQRI),浸出物與可提取物工作小組,《口服吸入藥和鼻科用藥中可提取物與浸出物的安全閥值與最佳實踐》,2006 年 11 月,http://www.pqri.org。
13. 美國食品和藥物管理局,聯邦法規第 21 篇第 170-199 部分,美國國家檔案文件管理局《聯邦公報》處;http://www.accessdata.fda.gov
14. 國際標準化組織 (ISO) 醫用裝置的生物學評估 -- 第 12 部分:樣本制備和參照材料;以及第 18 部分:材料化學特征的鑒定分析,http://www.iso.org
15. Hojnicki, P. 等等,《用于提取流程的一個系統性方法》,PDA研討會上發表;Extractable Puzzle,2005 年 5 月 22 日
16. Bart J.C J;《高分子添加劑分析》發表于《行業實踐與案例分析》,佛羅倫薩大學出版社,2006 年。
17. 產品質量研究所 (PQRI),浸出物與可提取物工作小組,《口服吸入藥和鼻科用藥中可提取物與浸出物的安全閥值與最佳實踐》,2006 年 11 月,http://www.pqri.org。
18. Changkang P. 等等,《封裝液體制劑中浸出物的識別方法》;《藥學與生物醫學分析雜志》,Elsevier B.V,2007 年。